Serialisierung für alle? Kennzeichnungspflicht von Arzneimittelverpackungen nimmt zu
Weltweit forcieren Pharmamärkte den Schutz ihrer Vertriebsketten. Zentrales Element ist die Verpackung, für die in immer mehr Ländern die individuelle Kennzeichnung zur Pflicht wird. Wie wirkt sich das auf die Zusammenarbeit zwischen Pharmaunternehmen und Verpacker aus?
Anbieter zum Thema
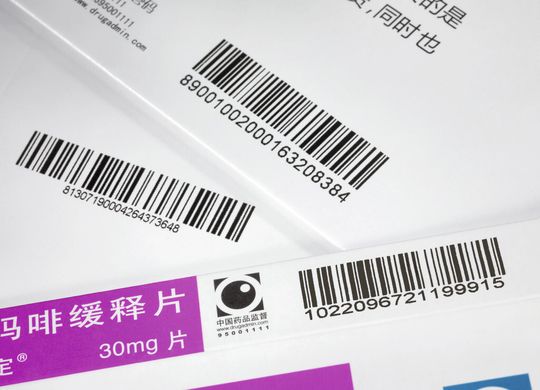
Die Serialisierung von Health-Care-Verpackungen rückt weltweit in den Vordergrund. Immer mehr Länder erlassen Vorschriften, bei ihnen vertriebene Arzneimittel mit individuellen Codes rückverfolgbar zu machen. Für die Unternehmen der Pharmaindustrie stehen damit weitreichende Änderungen der Prozessabläufe an. „Das stellt neue Anforderungen an die Zusammenarbeit zwischen Pharma- und Verpackungshersteller“, sagt Monika Schermanski, Vertriebsleiterin Pharma bei der internationalen Verpackungsgruppe Edelmann.
„Originalitätsschutz erfordert Konzepte, eine umfassende Beratung sowie prozessübergreifende Services. Pharma- und Verpackungshersteller müssen sich daher frühzeitig über die Einführung aller notwendigen Prozesse zum Erfüllen der Serialisierungs-Vorgaben abstimmen. Diese betreffen alle wichtigen Pharmamärkte.
Auch China zieht nach
Zu den bekanntesten gehört der US-Bundesstaat Kalifornien, der schon vor einigen Jahren das Anlegen eines „e-Pedigree“, also eines elektronischen „Stammbaums“ für Arzneimittel, verfolgt und ihn ab 2015 zur Pflicht macht. Schon bald soll eine für alle Bundesstaaten der USA geltende einheitliche Lösung am kalifornischen Gesetz ausgerichtet werden. Der genaue Zeitpunkt ist noch unbekannt.
Ebenfalls ab 2015 greift die Serialisierungsregel in China. Ab dann muss dort jede Arzneimittelverpackung einen individuellen Barcode enthalten. Hinter diesem steckt eine Seriennummer, die bei der chinesischen Behörde SFDA vorab beantragt und in deren Datenbank einzutragen ist.
Auch weitere Wachstumsmärkte wie Brasilien und Indien sowie Südkorea und Saudi-Arabien haben Vorschriften zur individuellen Kennzeichnung erlassen oder sind gerade dabei, dies zu tun. „In allen Fällen zeigt sich, dass die Vorgaben mit technischen und regulatorischen Umstellungen der Verpackungsprozesse verbunden sind, die Zeit und Ressourcen erfordern“, sagt Schermanski. „Es ist daher wichtig, das Thema Serialisierung frühzeitig anzugehen.“
(ID:42311404)





:quality(80)/p7i.vogel.de/wcms/ba/79/ba79d688575b69045de623fcc9c4a72c/0131450616v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/b4/9b/b49b69a3b9488a0279c4f77138c79e28/0131409269v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f6/47/f647d3034c38d029e48e9e4854d6d85f/0131310846v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/cc/07/cc074b31af47376cc7edffb120e6c8b5/0131265374v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/93/66/9366cfdcefc7d583896d26b8b7acecc0/0131232285v5.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/29/9f2988b96d1fc55d05934443b86083f9/0131195060v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/77/89/7789fae79ebe32f6a933d5800b51a026/0131191471v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/ca/f7/caf7ac2a1630095fde019eb9c20ff3e8/0131406800v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/24/ce/24cea247dc6b4fd93a0558be52cf549b/0131401769v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/44/86/44860f2d4fdd2a47b1c169d4f97b31ac/0131293698v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ef/7f/ef7f1e6cf60b0b7d00b918ca74fd6c47/0131242494v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8b/99/8b993138aae152c0e3446feb51008dcd/0131161698v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/43/fb/43fb7a19cde64296b2c32c06e913bc20/0130973263v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/34/61/3461df03788287428f0f8c4e72d79b36/0130972990v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/15/af/15af64322b6fc6e0114e838ea98375e7/0131255605v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e3/64/e364b14ca9094c2aa68f196ecd15701a/0131162486v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/2e/26/2e26282de9c432996615cda4d5e77745/0131193209v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/0f/35/0f3580c55e46869742e873d227ef38ca/0131426042v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/88/72/8872017e69cb8d75f3d457070ae7e4a0/0131417207v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/98/62/9862e760c7e6b764fff58602622aed9c/0131381014v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/31/fb/31fb4e265b356d45333585e4d170978d/0131311721v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/51/80/5180656d611925e506e2fd99aa1ae65f/0131443402v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/64/12/64126acac89347da2fcd59f1f01ed957/0131435860v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/9c/3e/9c3efa77d81ff979c693865cadaa9440/0131367221v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/fa/5d/fa5d896688b432f1a000dc4c5c5cabd5/0129619489v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/78/08/78082e2c5c40c2cf391113c8a9c42f97/0128109021v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/66/e1/66e19d7e4bf91b1e5a639daa038c3cd6/0129082515v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a5/90/a590eda77744612b7eacc2da0a0b2e84/0131400266v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6d/d4/6dd405b7fd94cec9053c7f7020f1164b/0130446154v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/10/25/1025a037607e7f48461124e5d58f13cb/0130577491v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/f3/df/f3dfb4f5ecc62eb26dbdff478f5decdb/0130484024v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a3/08/a308e4e4493fea16547dc727a06d0660/0131194785v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/f6/d1f6e4f7110c2eb680febb56e2c7e54f/0131181422v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/38/27/3827e393ab46ec720aa1ac7eb8b3b898/0131030092v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/cc/49/cc49c332d2acf742905f63b5ef02b6f3/0120324761v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ed/28/ed28176e6fb9e1dd42e7e0fff88db75b/0130199526v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8f/06/8f066870b3461f3d90c9f77d54b1a116/0130162998v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/75/097509e35ff7427a2d215577a951f9fc/0129978444v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/1e/7b1e69634150bb1caf42ae94b36f11ab/0130164126v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/36/38/3638c2c52566237bc7c3d8ae3d54aad6/0130163057v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/92/4d/924da0a1a22409425787c07395d56477/0130141086v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/111300/111318/65.png)
:fill(fff,0)/p7i.vogel.de/companies/62/98/62987c083933c/ness-w--rmetechnik-gmbh.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/17100/17177/65.jpg)
:quality(80)/p7i.vogel.de/wcms/50/3d/503dbecec6d5a01dee92da13ffcd6d97/0125654382v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/61/f9/61f97f676a01ca6501a4e12c04e6177b/0131072141v1.jpeg)