GMP als Time-to-Market-Faktor Warum Compliance bereits im Engineering entschieden wird
Anbieter zum Thema
Time-to-Market wird in Pharma-Projekten selten im Endspurt entschieden. Verzögerungen entstehen meist früh – im Engineering, in Spezifikationen, bei Lieferantenentscheidungen und im GMP-Verständnis. Wer Qualifizierung nur als Abnahme sieht, riskiert Nacharbeit und Dokumentationsstaus. Entscheidend ist ein Perspektivwechsel: „Design for Compliance“ wird zum Taktgeber.
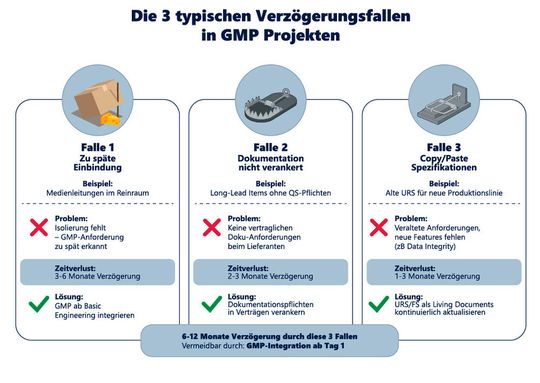
Ein Monteur steht im Reinraum, die Haube sitzt, das Werkzeug ist desinfiziert, die Uhr tickt. Der Lieferant meldet: „SAT abgeschlossen“. Das Projektteam ist zugeschaltet, QA ebenfalls. Doch der Qualifizierer widerspricht: „Durchgeführt ist nicht abgeschlossen. Abgeschlossen heißt dokumentiert, geprüft, freigegeben – mit letzter Unterschrift.“ Zwei Begriffe, die in vielen Projekten wie ein Synonym behandelt werden, entscheiden plötzlich über Wochen: Wird der Terminplan gehalten – oder rutscht der Produktionsstart?
Solche Situationen sind in pharmazeutischen Investitionsprojekten kein Ausnahmefall – sie zeigen ein strukturelles Problem. Time-to-Market wird nicht durch einen heroischen Sprint am Ende gewonnen, sondern in den vorgelagerten Projektphasen.
Melden Sie sich an oder registrieren Sie sich und lesen Sie weiter
Um diesen Artikel vollständig lesen zu können, müssen Sie registriert sein. Die kostenlose Registrierung bietet Ihnen Zugang zu exklusiven Fachinformationen.
Sie haben bereits ein Konto? Hier einloggen





:quality(80)/p7i.vogel.de/wcms/47/d1/47d1fd5605dd866a14d553e2e1cfca4b/0131498759v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ba/79/ba79d688575b69045de623fcc9c4a72c/0131450616v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/b4/9b/b49b69a3b9488a0279c4f77138c79e28/0131409269v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/cc/07/cc074b31af47376cc7edffb120e6c8b5/0131265374v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/93/66/9366cfdcefc7d583896d26b8b7acecc0/0131232285v5.jpeg)
:quality(80)/p7i.vogel.de/wcms/9f/29/9f2988b96d1fc55d05934443b86083f9/0131195060v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/77/89/7789fae79ebe32f6a933d5800b51a026/0131191471v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/ca/f7/caf7ac2a1630095fde019eb9c20ff3e8/0131406800v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/24/ce/24cea247dc6b4fd93a0558be52cf549b/0131401769v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/44/86/44860f2d4fdd2a47b1c169d4f97b31ac/0131293698v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/36/5f/365f6cad20a2b928e61d848d90748f79/0131529707v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/0d/f2/0df23262da54bcd8ec71ff1461d019c9/0131478820v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/ef/7f/ef7f1e6cf60b0b7d00b918ca74fd6c47/0131242494v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8b/99/8b993138aae152c0e3446feb51008dcd/0131161698v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ec/b4/ecb42cf1ae88a29fb4397ab6325a0b86/0131587044v5.jpeg)
:quality(80)/p7i.vogel.de/wcms/15/af/15af64322b6fc6e0114e838ea98375e7/0131255605v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/0c/f4/0cf401eea868c54476f23dd5428ddb76/0131582924v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c9/c4/c9c4d8ca7acbbc591be0060038f43b29/0131566065v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c6/ee/c6eebd1d13c1f268b616efb60c2641b9/0131339764v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/11/a8/11a816b41bbf272c41a62bed104a79cf/0131506833v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/51/80/5180656d611925e506e2fd99aa1ae65f/0131443402v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/64/12/64126acac89347da2fcd59f1f01ed957/0131435860v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/9c/3e/9c3efa77d81ff979c693865cadaa9440/0131367221v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/fa/5d/fa5d896688b432f1a000dc4c5c5cabd5/0129619489v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/78/08/78082e2c5c40c2cf391113c8a9c42f97/0128109021v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/66/e1/66e19d7e4bf91b1e5a639daa038c3cd6/0129082515v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/e5/e1/e5e14451ca515fdcd285deddc09c730c/0131557920v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a5/90/a590eda77744612b7eacc2da0a0b2e84/0131400266v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/6d/d4/6dd405b7fd94cec9053c7f7020f1164b/0130446154v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a3/08/a308e4e4493fea16547dc727a06d0660/0131194785v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d1/f6/d1f6e4f7110c2eb680febb56e2c7e54f/0131181422v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/38/27/3827e393ab46ec720aa1ac7eb8b3b898/0131030092v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/cc/49/cc49c332d2acf742905f63b5ef02b6f3/0120324761v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ed/28/ed28176e6fb9e1dd42e7e0fff88db75b/0130199526v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8f/06/8f066870b3461f3d90c9f77d54b1a116/0130162998v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/75/097509e35ff7427a2d215577a951f9fc/0129978444v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/7b/1e/7b1e69634150bb1caf42ae94b36f11ab/0130164126v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/36/38/3638c2c52566237bc7c3d8ae3d54aad6/0130163057v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/92/4d/924da0a1a22409425787c07395d56477/0130141086v2.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/2000/2093/65.jpg)
:fill(fff,0)/p7i.vogel.de/companies/69/5b/695b8e4976caa/40jahre-denios-logo-srgb-web.svg)
:fill(fff,0)/p7i.vogel.de/companies/68/f6/68f632f26ee6b/handshake-logo-png.png)
:quality(80)/p7i.vogel.de/wcms/3a/62/3a62e7ceb8e66e53dc9172da0db201b2/0128830829v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f4/d6/f4d61d0a93f4e9a0e4177073fd0815af/0129922670v6.jpeg)