Arzneimittelfälschung Mit Serialisierung Arzneimittelfälschungen verhindern
Die Richtlinie der Europäischen Union zur Verbesserung des Fälschungsschutzes von Arzneimitteln in der Supply Chain ist seit Juli in Kraft. Pharmazeutische Hersteller müssen künftig alle betroffenen Arzneimittel mit einem Code mit eindeutiger, zufälliger Seriennummer bedrucken. Der Weg dorthin ist komplex und nicht ohne Hürden.
Anbieter zum Thema
Die Europäische Union hat am 1. Juli 2011 die seit längerer Zeit diskutierte Richtlinie 2011/62/EU zur Bekämpfung von Arzneimittelfälschungen im EU-Amtsblatt veröffentlicht. Somit ist der Startschuss für eine EU-weite Lösung zur Fälschungssicherheit auf dem Pharmamarkt gefallen. Die EU-Richtlinie regelt maßgeblich, dass rezeptpflichtige Arzneimittel künftig Sicherheitsmerkmale tragen müssen, welche eine Echtheitsprüfung entlang der kompletten Lieferkette ermöglichen. Daher sind auch sämtliche Marktteilnehmer, von den pharmazeutischen Unternehmen und den von ihnen beauftragten Lohnherstellern über den Großhandel bis hin zu den Apotheken, in das Lösungskonzept integriert.
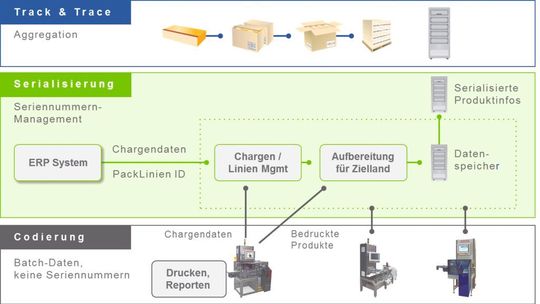
Arzneimittel werden künftig unionsweit harmonisierte Sicherheitsmerkmale tragen, sodass gefälschte Arzneimittel erkannt und aus dem Verkehr gezogen werden können. Die europäischen Dachverbände der forschenden Arzneimittelhersteller (efpia), des Großhandels (GIRP) und der Apotheker (PGEU) befürworten dazu eine eindeutige Kennzeichnung jeder Verkaufsverpackung per Serialisierung mittels maschinenlesbarem 2D-Matrix-Code.
Die Echtheitsprüfung über einen Vergleich der im Data-Matrix-Code enthaltenen Information mit dem in einer zentralen Datenbank gespeicherten Datensatz wird im Rahmen der Medikamentenabgabe in der Apotheke erfolgen. Auch weitere Marktpartner können diesen Abgleich bei Bedarf durchführen. Um sicher zu stellen, dass nicht nur die Verpackung eines Produktes auf diese Weise geschützt ist, sondern auch ihr Inhalt, sieht die Richtlinie als ergänzende Sicherheitsmaßnahme die Ausstattung der Packungen mit einem Originalitätsverschluss vor (Tamper evident packaging).
Der Endtermin für die EU-weite Fertigstellung ist von der Europäischen Kommission zwar bis heute noch nicht auf einen festen Stichtag datiert worden, jedoch ist das Zeitfenster absehbar: Geplant ist der Aufbau des Verifikationssystems spätestens bis 2016.
Lesen Sie weiter auf Seite 2, welche Hürden es bei der Umsetzung gibt
(ID:28810840)





:quality(80)/p7i.vogel.de/wcms/97/15/9715bd07da9c856f2c341db46ba57888/0130056361v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9c/a5/9ca50150322422c2f5867ab2a4e2f744/0130054833v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/65/c5/65c52be35edd449b6e87f2ef0ca10666/0130022649v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/91/d0/91d001d88bdc0eb4b9437b089ee1623d/0129998092v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/b7/8d/b78d9dedb1179fa019ed5699ca639c78/0129960056v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/b6/c2/b6c2024000a187c9c801112f20f913d9/0129896948v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/59/52/595203df195edbc7091bbad75984c155/0129590988v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/79/fb/79fbc8c7aedbd4a7dda0f11756fa8239/0129836447v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cf/09/cf0975f2fcf6be2d8c3a4ed786674e7f/0129560848v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/23/f3/23f361183c09d9d63c2c5bd81a829c73/0129516512v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/1f/42/1f42bb94b56e2b09ba30f333b6c599d8/0129813641v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/6f/16/6f1682e8494b6b1530bbcc837082b7b1/0129984412v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/3f/33/3f33a239d61d8cb49bf163b361bdf973/0129978032v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/f4/84/f4848e8c2e3c09a98fccec56a942f827/0129812476v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a7/00/a7002f36fb7e57a5ed31bed86018be6d/0130061185v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/9e/f2/9ef2d96d6306280efd7c300c4ee88d73/0129541164v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/68/5b/685bc646346ac5cb39ede42ec6fe1ac3/0129990711v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/07/da/07da7c8dadb0c46b1592a588ee65bd0f/0130028009v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/b2/4e/b24e9a0b4c8432357a25153dfbcc17cb/0129801012v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/f4/d6/f4d61d0a93f4e9a0e4177073fd0815af/0129922670v6.jpeg)
:quality(80)/p7i.vogel.de/wcms/38/72/3872035e79d44795ff46bd8b0f9e1d5b/0129912318v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/f5/20/f520bbf084e5b35f0e8d68ede0f2b675/0129967379v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/82/1f/821fc3e325fe033a4184b4053d3d3d42/0129557944v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/4c/d6/4cd6446e617bccb1c4898b3e055e73e6/0129620835v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/fa/5d/fa5d896688b432f1a000dc4c5c5cabd5/0129619489v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/78/08/78082e2c5c40c2cf391113c8a9c42f97/0128109021v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/66/e1/66e19d7e4bf91b1e5a639daa038c3cd6/0129082515v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/a0/49/a0491a8033db3d6dea79af80eadca57b/0129938820v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/22/08/2208b1ce309844d3d7b269715cadf0ed/0129830281v4.jpeg)
:quality(80)/p7i.vogel.de/wcms/0f/06/0f066fd5f1e3706dcb972847c50be66c/0130035069v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/44/8b/448b006c96b1442ad868a8150b3b6879/0130032961v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/3e/9f/3e9f1fd97b266500fdc9741250b0f3a4/0130022072v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/09/75/097509e35ff7427a2d215577a951f9fc/0129978444v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/a5/9e/a59e9628e2c8ea914f63f82989dc062d/0129242430v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8a/a1/8aa1cd7e3e60e8b6608f134cc51b2c8d/0128367970v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/aa/e2/aae2a5f31ce042c47f08284db85e9b33/0129792914v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/7c/3a/7c3a35a23adfc4dc53b81555b714304b/0109473810v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/71/b4/71b43f5588655bf89cbc3faeb311ea78/0126955685v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/9a/d9/9ad99104c6f6685d534af0dbef9c0ace/0126730715v1.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/63/d1/63d102a099f51/logo.jpeg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/27600/27667/65.jpg)
:fill(fff,0)/images.vogel.de/vogelonline/companyimg/45900/45920/65.jpg)
:quality(80)/p7i.vogel.de/wcms/92/af/92afd07f85af1514f50e53856012286c/0124405656v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/50/3d/503dbecec6d5a01dee92da13ffcd6d97/0125654382v2.jpeg)